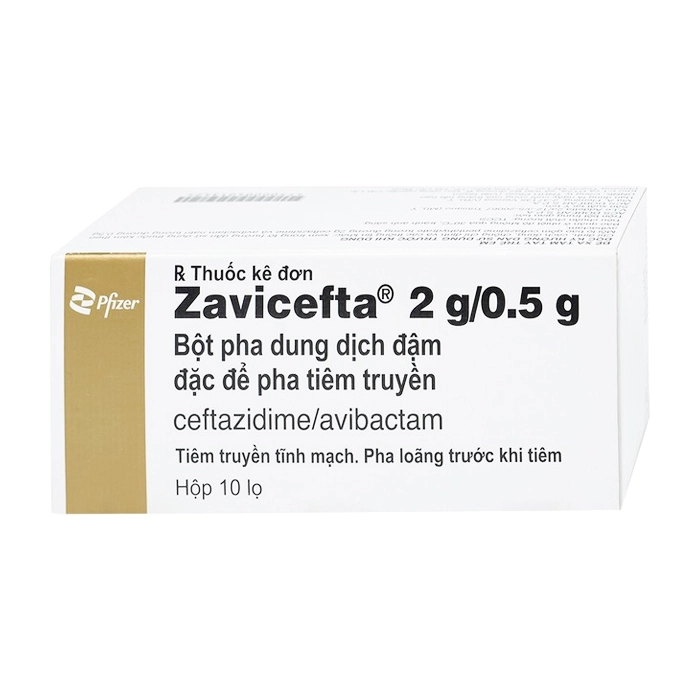
Zavicefta 2g/0.5g Pfizer 10 lọ
* Hình sản phẩm có thể thay đổi theo thời gian
** Giá sản phẩm có thể thay đổi tuỳ thời điểm
30 ngày trả hàng Xem thêm

Số đăng ký: 800110440223
Cách tra cứu số đăng ký thuốc được cấp phépTìm thuốc Ceftazidime/Avibactam khác
Tìm thuốc cùng thương hiệu Pfizer khác
Thuốc này được bán theo đơn của bác sĩ
Gửi đơn thuốc.svg)
Bạn muốn nhận hàng trước 4h hôm nay. Đặt hàng trong 55p tới và chọn giao hàng 2H ở bước thanh toán. Xem chi tiết
Thông tin sản phẩm
| Số đăng ký: | 800110440223 |
| Hoạt chất: | |
| Quy cách đóng gói: | |
| Thương hiệu: | |
| Xuất xứ: | |
| Thuốc cần kê toa: | |
| Dạng bào chế: | |
| Hàm Lượng: | |
| Nhà sản xuất: | |
| Tiêu chuẩn: |
Nội dung sản phẩm
Thành phần
- Ceftazidime: 2g
- Avibactam: 0.5g
Công dụng (Chỉ định)
Ở người lớn, Zavicefta được chỉ định để điều trị các nhiễm trùng sau:
- Nhiễm trùng ổ bụng có biến chứng
- Nhiễm trùng tiết niệu phức tạp, bao gồm viêm thận – bể thận
- Viêm phổi mắc phải tại bệnh viện, bao gồm viêm phổi liên quan đến thở máy
- Zavicefta cũng được chỉ định để điều trị các nhiễm trùng gây ra bởi vi khuẩn Gram âm hiếu khí ở bệnh nhân trưởng thành có ít lựa chọn điều trị.
- Cần xem xét thêm các hướng dẫn chính thức về việc sử dụng kháng sinh hợp lý.
Liều dùng
Khuyến nghị chỉ nên sử dụng Zavicefta để điều trị nhiễm trùng do vi khuẩn Gram âm hiếu khí ở bệnh nhân trưởng thành có ít lựa chọn điều trị sau khi tham khảo ý kiến bác sĩ có kinh nghiệm trong xử trí các bệnh truyền nhiễm
Bảng 1 trình bày liều tiêm truyền tĩnh mạch khuyến nghị cho bệnh nhân có độ thanh thải creatinine ước tính (CrCL) ≥ 51mL/phút
Bảng 1 Liều tiêm truyền tĩnh mạch khuyến nghị cho bệnh nhân có CrCL ước tính ≥ 51mL/phút:

- CrCL được ước tính bằng công thức Cockcroft-Gault
- Sử dụng kết hợp với metronidazole khi đã biết hoặc nghi ngờ có tác nhân gây bệnh kỵ khí góp phần vào quá trình nhiễm khuẩn
- Sử dụng kết hợp với một chất kháng khuẩn có hoạt tính kháng các tác nhân gây bệnh Gram dương khi đã biết hoặc nghi ngờ các tác nhân này góp phần vào quá trình nhiễm khuẩn
- Tổng thời gian điều trị có thể bao gồm Zavicefta tiêm truyền tĩnh mạch được tiếp nối bằng liệu pháp đường uống thích hợp
- Có rất ít kinh nghiệm với việc sử dụng Zavicefta dài hơn 14 ngày
Các nhóm đối tượng đặc biệt
Người cao tuổi:
- Không cần điều chỉnh liều ở bệnh nhân cao tuổi (xem mục 5.2).
Suy thận:
- Không cần điều chỉnh liều ở bệnh nhân suy thận nhẹ (CrCL ước tính ≥ 51 – ≤ 80 mL/phút ) (xem mục 5.2).
Bảng 2 trình bày các điều chỉnh liều khuyến nghị cho bệnh nhân có CrCL ước tính ≤ 50 mL/phút (xem các mục 4.4 và 5.2).
Bảng 2 Liều tiêm truyền tĩnh mạch khuyến nghị cho bệnh nhân có CrCL ước tính ≤ 50 mL/phút:

CrCL được ước tính bằng công thức Cockcroft-Gault
- Các khuyến nghị liều dựa trên mô hình dược động học
- Ceftazidime và avibactam có thể loại bỏ bằng cách thẩm tách máu (xem các mục 4.9 và 5.2).
Vào những ngày thẩm tách máu, cần cho dùng ceftazidime-avibactam sau khi đã thẩm tách máu.
Suy gan: Không cần điều chỉnh liều ở bệnh nhân suy gan:
Bệnh nhân nhi:
- Tính an toàn và hiệu quả ở trẻ em và trẻ vị thành niên dưới 18 tuổi chưa được thiết lập.
- Dữ liệu hiện có được mô tả trong mục 4.8 nhưng không thể đưa ra khuyến nghị về liều dùng.
Cách dùng
Thuốc được dùng qua đường truyền tĩnh mạch trong 120 phút với thể tích truyền là 100 mL.
Lưu ý đặc biệt khi loại bỏ và các xử lý khác:
Bột phải được hoàn nguyên với nước pha tiêm và sau đó dung dịch cô đặc thu được phải được pha loãng ngay trước khi sử dụng. Dung dịch đã hoàn nguyên là một dung dịch màu vàng nhạt, không có bất kỳ tiểu phân lạ nào.
Cần sử dụng kỹ thuật vô trùng chuẩn để chuẩn bị và tiêm truyền dung dịch.
- Đưa kim tiêm qua nút lọ và tiêm vào 10 ml nước vô khuẩn pha tiêm .
- Rút kim và lắc lọ để tạo ra một dung dịch trong suốt.
- Không được đưa kim rút khí vào cho đến khi thuốc đã hòa tan. Đưa kim rút khí qua nút lọ để giảm áp lực bên trong.
- Chuyển toàn bộ dung dịch đã pha (khoảng 12,0 ml) vào một túi truyền ngay lập tức.
Có thể giảm liều bằng cách chuyển một thể tích dung dịch đã pha thích hợp vào một túi truyền, căn cứ vào hàm lượng ceftazidime và avibactam lần lượt là 167,3 mg/ml và 41,8 mg/ml. Có thể đạt được liều 1000 mg/250 mg hoặc 750 mg/187,5 mg lần lượt với thể tích 6,0 ml hoặc 4,5 ml.
Ghi chú: Để bảo đảm độ vô trùng của thuốc, điều quan trọng là không được đưa kim rút khí qua nút đóng lọ trước khi thuốc tan hoàn toàn
Các lọ bột ceftazidime-avibactam cần được hoàn nguyên với 10 ml nước vô khuẩn pha tiêm, sau đó lắc cho đến khi tan hoàn toàn các thành phần. Túi truyền có thể có bất kỳ thành phần nào sau đây: dung dịch natri chloride 9 mg/ml (0,9%) pha tiêm, dung dịch dextrose 50 mg/ml (5%) pha tiêm, dung dịch natri chloride 4,5 mg/ml và dextrose 25 mg/ml pha tiêm (0,45% natri chloride và 2,5% dextrose) hoặc dung dịch Lactated Ringer. Có thể sử dụng túi truyền 100 ml để chuẩn bị dung dịch truyền, dựa vào thể tích tiêm cần cho mỗi bệnh nhân. Tổng thời gian từ khi bắt đầu hoàn nguyên và hoàn tất việc chuẩn bị dung dịch truyền tĩnh mạch không được quá 30 phút.
Mỗi lọ chỉ dùng một lần.
Bất kỳ phần thuốc nào không sử dụng hoặc chất thải nào cũng phải được thải bỏ theo quy định của địa phương.
Quá liều
- Dùng quá liều ceftazidime/avibactam có thể dẫn đến di chứng thần kinh bao gồm bệnh não, co giật và hôn mê, do thành phần ceftazidime.
- Có thể giảm nồng độ ceftazidime trong huyết thanh bằng cách thẩm tách máu hoặc thẩm phân phúc mạc. Trong 4 giờ thẩm tách máu, 55% liều avibactam được loại bỏ.
Không sử dụng trong trường hợp sau (Chống chỉ định)
- Quá mẫn với hoạt chất hoặc bất kỳ thành phần tá dược nào liệt kê ở mục 6.1.
- Quá mẫn với bất kỳ kháng sinh nào thuộc nhóm cephalosporin.
- Quá mẫn nặng (ví dụ: phản ứng phản vệ, phản ứng nặng trên da) với bất kỳ kháng sinh nào khác thuộc nhóm β-lactam (ví dụ: penicillin, monobactam hoặc carbapenem).
Tác dụng không mong muốn (Tác dụng phụ)
Tóm tắt đặc tính an toàn:
Trong bảy nghiên cứu lâm sàng Pha 2 và Pha 3, 2024 bệnh nhân trưởng thành đã được điều trị bằng Zavicefta. Các phản ứng bất lợi thường gặp nhất xảy ra ở ≥5% bệnh nhân được điều trị bằng Zavicefta là dương tính với nghiệm pháp Coombs trực tiếp, buồn nôn và tiêu chảy. Buồn nôn và tiêu chảy thường ở mức độ nhẹ hoặc vừa.
Bảng danh sách các phản ứng bất lợi:
Các phản ứng bất lợi sau đây đã được báo cáo khi dùng ceftazidime đơn độc và/hoặc được xác định trong các thử nghiệm Pha 2 và Pha 3 với Zavicefta. Các phản ứng bất lợi được phân loại theo tần suất và hệ cơ quan. Các phân loại tần suất bắt nguồn từ các phản ứng bất lợi và/hoặc các bất thường xét nghiệm có thể có ý nghĩa về mặt lâm sàng, và được xác định theo các quy ước sau đây:
Rất thường gặp (≥1/10)
Thường gặp (≥1/100 và <1/10)
Ít gặp (≥1/1000 và <1/100)
Hiếm gặp (≥1/10.000 và <1/1000)
Rất hiếm gặp (<1/10.000)
Chưa rõ (không thể ước tính từ dữ liệu có sẵn)
Bảng 3 Tần suất của các phản ứng bất lợi theo phân loại hệ cơ quan:
Nhiễm trùng và nhiễm ký sinh trùng:
- Thường gặp: Nhiễm nấm Candida (bao gồm nhiễm nấm Candida âm hộ – âm đạo và nhiễm nấm Candida miệng)
- Ít gặp: Viêm đại tràng do Clostridium difficile Viêm đại tràng giả mạc
Rối loạn máu và hệ bạch huyết:
- Rất thường gặp: Dương tính với nghiệm pháp Coombs trực tiếp
- Thường gặp: Tăng bạch cầu ưa eosin, Tăng tiểu cầu, Giảm tiểu cầu
- Ít gặp: Giảm bạch cầu trung tính, Giảm bạch cầu, Tăng bạch cầu
- Chưa rõ: Giảm bạch cầu hạt, Thiếu máu tán huyết
Rối loạn hộ miễn dịch:
- Chưa rõ: Phản ứng phản vệ
Rối loạn hộ thần kinh:
- Thường gặp: Đau đầu, Chóng mặt
- Ít gặp: Dị cảm
Rối loạn tiêu hóa:
- Thường gặp: Tiêu chảy, Đau bụng, Buồn nôn, Nôn
- Ít gặp: Rối loạn vị giác
Rối loạn gan mật:
- Thường găp: Tăng alanine aminotransferase, Tăng aspartate aminotransferase, Tăng phosphatase kiềm trong máu. Tăng gammaglutamyltransfer ase, Tăng lactate dehydrogenase trong máu
- Chưa rõ: Vàng da
Rối loạn da và mô dưới da:
- Thường gặp: Ban dát sần, Nổi mề đay, Ngứa
- Chưa rõ: Hoại tử biểu bì nhiễm độc, Hội chứng StevensJohnson, Hồng ban đa dạng, Phù mạch, Phản ứng thuốc có tăng bạch cầu ưa cosin và các triệu chứng toàn thân (Drug Reaction with Eosinophilia and Systemic Symptoms – DRESS)
Rối loạn thận và tiết niệu:
- Ít gặp: Tăng creatinine máu, Tăng ure máu, Suy thận cấp
- Rất hiếm gặp: Viêm ống thận thận mô kẽ
Rối loạn chung và tình trạng tại nơi sử dụng thuốc:
- Thường gặp: Huyết khối tại nơi truyền thuốc viêm tĩnh mạch tại nơi truyền thuốc Sốt
Bệnh nhân nhi:
- Đánh giá tính an toàn ở trẻ em dựa trên dữ liệu về tính an toàn từ 1 nghiên cứu trong đó 61 bệnh nhân nhi từ 3 đến dưới 18 tuổi bị nhiễm trùng ổ bụng có biến chứng đã được cho dùng Zavicefta. Nhìn chung, tính an toàn ở 61 bệnh nhân này tương tự với kết quả quan sát được ở nhóm đối tượng trưởng thành bị nhiễm trùng ổ bụng có biến chứng.
Thông báo cho bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
Tương tác với các thuốc khác
In vitro, avibactam là một cơ chất của chất vận chuyển OAT1 và OAT3, điều này có thể góp phần vào sự hấp thu chủ động avibactam từ máu, và do đó ảnh hưởng đến sự thải trừ của thuốc. Probenecid (một chất ức chế OAT mạnh) ức chế sự hấp thu này từ 56% đến 70% in vitro, và vì vậy có khả năng thay đổi sự thải trừ avibactam. Do nghiên cứu lâm sàng về sự tương tác giữa avibactam và probenecid chưa được tiến hành, không khuyến nghị dùng đồng thời avibactam với probenecid.
Avibactam không cho thấy sự ức chế đáng kể đối với các enzym cytochrome P450 in vitro. Avibactam và ceftazidime không thể hiện sự cảm ứng cytochrome P450 in vitro với các nồng độ liên quan trên lâm sàng. Avibactam và ceftazidime không ức chế các chất vận chuyển chính trong gan và thận trong phạm vi phơi nhiễm tương ứng trên lâm sàng, vì vậy khả năng tương tác qua cơ chế này được xem là thấp.
Dữ liệu lâm sàng đã cho thấy không có tương tác giữa ceftazidime và avibactam, và giữa ceftazidime/avibactam và metronidazole.
Các dạng tương tác khác:
- Điều trị đồng thời với cephalosporin liều cao và các thuốc gây độc thận, chẳng hạn như các aminoglycoside hoặc các thuốc lợi tiểu mạnh (ví dụ: furosemide) có thể ảnh hưởng bất lợi lên chức năng thận (xem mục 4.4).
- Chloramphenicol có tính đối kháng in vitro với ceftazidime và các cephalosporin khác.
- Sự tương quan lâm sàng của phát hiện này chưa được biết, nhưng do khả năng đối kháng in vivo nên cần tránh sử dụng kết hợp thuốc này.
Lưu ý khi sử dụng (Cảnh báo và thận trọng)
Phản ứng quá mẫn:
- Có thể xảy ra phản ứng quá mẫn nghiêm trọng và đôi khi gây tử vong (xem các mục 4.3 và 4.8). Trong trường hợp xảy ra phản ứng quá mẫn, phải ngay lập tức ngừng điều trị bằng Zavicefta và phải tiến hành các biện pháp cấp cứu thích hợp.
- Trước khi bắt đầu điều trị, cần tìm hiểu xem bệnh nhân có tiền sử bị phản ứng quá mẫn với ceftazidime, với các cephalosporin khác hay với bất kỳ loại chất kháng khuẩn nào khác thuộc nhóm β-lactam hay không. Cần thận trọng nếu ceftazidime/avibactam được sử dụng ở bệnh nhân có tiền sử quá mẫn ở mức độ không nghiêm trọng với penicillin, monobactam hoặc carbapenem.
Tiêu chảy do Clostridium difficile:
- Đã có báo cáo tiêu chảy do Clostridium difficile với ceftazidime/avibactam, và có thể có phạm vi cấp độ từ nhẹ đến đe dọa tính mạng. Cần cân nhắc chẩn đoán này ở bệnh nhân có biểu hiện tiêu chảy trong hoặc sau khi cho dùng Zavicefta (xem mục 4.8). Cần cân nhắc ngừng điều trị bằng Zavicefta và tiến hành biện pháp điều trị đặc hiệu với Clostridium difficile. Không được dùng thuốc ức chế nhu động.
Suy thận:
- Ceftazidime và avibactam được thải trừ qua thận, do đó, cần giảm liều theo mức độ suy thận (xem mục 4.2). Di chứng thần kinh, bao gồm run, rung giật cơ, động kinh không co giật, co giật, bệnh não và hôn mê đôi khi được báo cáo với ceftazidime khi không giảm liều ở bệnh nhân suy thận. Ở bệnh nhân suy thận, nên theo dõi chặt chẽ độ thanh thải creatinine ước tính. Ở một số bệnh nhân, độ thanh thải creatinine được ước tính từ creatinine trong huyết thanh có thể thay đổi nhanh chóng, đặc biệt là ở giai đoạn đầu quá trình điều trị nhiễm trùng.
Độc tính trên thận:
- Điều trị đồng thời với cephalosporin liều cao và các thuốc gây độc cho thận như các aminoglycoside hoặc thuốc lợi tiểu mạnh (ví dụ: furosemide) có thể gây ảnh hưởng bất lợi lên chức năng thận.
- Xét nghiệm kháng globulin trực tiếp (nghiệm pháp DAGT hay Coombs) chuyển đổi huyết thanh và nguy cơ thiếu máu tán huyết tiềm ẩn
- Sử dụng ceftazidime/avibactam có thể tạo ra kết quả dương tính trong xét nghiệm kháng globulin trực tiếp (nghiệm pháp DAGT hay Coombs), có thể ảnh hưởng tới kết quả phản ứng chéo của máu và/hoặc có thể gây thiếu máu tán huyết miễn dịch do thuốc gây ra (xem mục 4.8). Trong khi chuyển đổi huyết thanh DAGT ở bệnh nhân đang dùng Zavicefta thường gặp trong các thử nghiệm lâm sàng (khoảng chuyển đổi huyết thanh ước tính trong các nghiên cứu Pha 3 là từ 3,2% đến 20,8% ở bệnh nhân có kết quả âm tính với nghiệm pháp Coombs vào lúc ban đầu và ít nhất một xét nghiệm theo dõi), không có bằng chứng tán huyết ở bệnh nhân có DAGT dương tính khi điều trị.
- Tuy nhiên, không thể loại trừ khả năng thiếu máu tán huyết có thể xảy ra liên quan đến điều trị bằng Zavicefta. Bệnh nhân bị thiếu máu trong khi hoặc sau khi điều trị bằng Zavicefta cần được đánh giá về khả năng này.
Các giới hạn của dữ liệu lâm sàng:
- Các nghiên cứu xác định tính hiệu quả và an toàn lâm sàng của Zavicefta đã được tiến hành ở bệnh nhân nhiễm trùng ổ bụng có biến chứng, nhiễm trùng tiết niệu phức tạp và viêm phổi mắc phải tại bệnh viện (bao gồm viêm phổi liên quan đến thở máy).
Nhiễm trùng ổ bụng có biến chứng:
- Trong hai nghiên cứu ở bệnh nhân nhiễm trùng ổ bụng có biến chứng, chẩn đoán thường gặp nhất (khoảng 42%) là thủng ruột thừa hoặc áp-xe quanh ruột thừa. Khoảng 87% bệnh nhân có điểm số APACHE II ≤ 10 và 4,0% bị nhiễm khuẩn huyết ở lần khám cơ bản. Tử vong xảy ra ở 2,1% (18/857) bệnh nhân đã dùng Zavicefta và metronidazole và ở 1,4% (12/863) bệnh nhân đã dùng meropenem.
- Trong một phân nhóm với CrCL ban đầu từ 30 đến 50 mL/phút, tử vong xảy ra ở 16,7% (9/54) bệnh nhân đã dùng Zavicefta và metronidazole và ở 6,8% (4/59) bệnh nhân đã dùng meropenem. Các bệnh nhân có CrCL từ 30 đến 50 mL/phút đã dùng liều Zavicefta thấp hơn liều hiện được khuyến nghị ở phân nhóm này.
Nhiễm trùng tiết niệu phức tạp:
- Trong hai nghiên cứu trên bệnh nhân nhiễm trùng tiết niệu phức tạp, 381/1091 (34,9%) bệnh nhân được thu nhận bị nhiễm trùng tiết niệu phức tạp không có viêm thận-bể thận trong khi 710 (65,1%) bệnh nhân được thu nhận bị viêm thận-bể thận cấp tính (nhóm đối tượng theo ý định điều trị (Modified Intent to Treat – mMITT). Tổng cộng có 81 bệnh nhân mắc nhiễm trùng tiết niệu phức tạp (7,4%) bị nhiễm khuẩn huyết ở lần khám ban đầu.
Viêm phổi mắc phải tại bệnh viện, bao gồm viêm phổi liên quan đến thở máy:
- Trong một nghiên cứu ở bệnh nhân bị viêm phổi mắc phải tại bệnh viện, 280/808 (34,7%) người bị viêm phổi liên quan đến thở máy và 40/808 (5,0%) người bị nhiễm khuẩn huyết ở lần khám ban đầu.
Bệnh nhân có ít lựa chọn điều trị:
- Việc sử dụng ceftazidime/avibactam để điều trị cho bệnh nhân bị nhiễm trùng do các tác nhân gây bệnh hiếu khí Gram âm có ít lựa chọn điều trị cần dựa trên kinh nghiệm với ceftazidime đơn trị và các phân tích tương quan dược động học-dược lực học với ceftazidime/avibactam (xem mục 5.1).
Phổ hoạt tính của ceftazidime/avibactam:
- Ceftazidime có ít hoặc không có hoạt tính kháng lại phần lớn các vi khuẩn Gram dương và vi sinh vật kỵ khí (xem các mục 4.2 và 5.1). Cần sử dụng thêm các chất kháng khuẩn khác khi đã biết hoặc nghi ngờ những tác nhân này góp phần vào quá trình nhiễm khuẩn.
- Phổ ức chế của avibactam bao gồm nhiều enzym bất hoạt ceftazidime, bao gồm các β-lactamase nhóm A và β-lactamase nhóm C theo phân loại Ambler. Avibactam không ức chế các enzym nhóm B (metallo-β-lactamase) và không có khả năng ức chế vài enzym nhóm D (xem mục 5.1).
Các vi sinh vật không nhạy cảm với thuốc:
- Sử dụng trong thời gian dài có thể dẫn đến phát triển quá mức các vi sinh vật không nhạy cảm với thuốc (ví dụ: enterococci, nấm), có thể cần tạm ngưng điều trị hoặc sử dụng các biện pháp thích hợp khác.
Ảnh hưởng lên các xét nghiệm:
- Ceftazidime có thể gây nhiễu các xét nghiệm sử dụng các phương pháp khử đồng (Benedict’s, Fehling’s, Clinitest) để phát hiện glucose niệu dẫn đến kết quả dương tính giả. Ceftazidime không gây ảnh hưởng đến các xét nghiệm dựa trên enzym để phát hiện glucose niệu.
Chế độ ăn kiểm soát natri:
- Mỗi lọ có chứa tổng cộng khoảng 6,37 mmol natri (khoảng 146 mg), tương đương với 7,3% mức tiêu thụ natri tối đa hàng ngày mà WHO khuyến nghị. Liều hàng ngày tối đa của thuốc này tương đương với 22% mức tiêu thụ natri tối đa hàng ngày mà WHO khuyến nghị.
- Phải cân nhắc yếu tố này khi sử dụng Zavicefta ở bệnh nhân đang dùng chế độ ăn kiểm soát natri.
Phụ nữ mang thai và cho con bú
Phụ nữ mang thai:
- Các nghiên cứu trên động vật với ceftazidime không cho thấy tác động có hại trực tiếp hay gián tiếp đối với thai kì, sự phát triển của phôi/bào thai, quá trình sinh đẻ hoặc sự phát triển sau sinh. Các nghiên cứu trên động vật với avibactam đã cho thấy độc tính sinh sản mà không có bằng chứng về tác dụng gây quái thai.
- Chỉ nên sử dụng ceftazidime/avibactam trong khi mang thai nếu lợi ích tiềm tàng lớn hơn nguy cơ có thể có.
Phụ nữ cho con bú:
- Ở người, ceftazidime có bài tiết vào sữa mẹ với lượng nhỏ. Không rõ avibactam có tiết vào sữa mẹ ở người hay không. Không thể loại trừ nguy cơ cho trẻ sơ sinh/trẻ nhũ nhi. Phải đưa ra quyết định có ngừng cho con bú hay ngừng/kiêng điều trị bằng ceftazidime/avibactam, cân nhắc đến lợi ích của việc cho con bú đối với đứa trẻ và lợi ích của việc điều trị đối với người mẹ.
Khả năng sinh sản:
- Ảnh hưởng của ceftazidime/avibactam lên khả năng sinh sản ở người chưa được nghiên cứu. Không có dữ liệu về các nghiên cứu trên động vật với ceftazidime. Các nghiên cứu trên động vật với avibactam không cho thấy tác dụng có hại đối với khả năng sinh sản.
Người lái xe và vận hành máy móc
- Các tác dụng không mong muốn có thể gặp (ví dụ: chóng mặt) có thể gây ảnh hưởng đến khả năng lái xe và sử dụng máy móc sau khi dùng Zavicefta.
Bảo quản
- Nơi khô, tránh ánh sáng, nhiệt độ dưới 30°C.
Đánh Giá - Bình Luận
- Đặt đơn thuốc trong 30 phút. Gửi đơn
- Giao nhanh 2H nội thành HCM Chính sách giao hàng 2H.
- Mua 1 tặng 1 Đông Trùng Hạ Thảo Famitaa. Xem ngay
- Mua Combo giá tốt hơn. Ghé ngay
- Miễn phí giao hàng cho đơn hàng 700K
- Đổi trả trong 6 ngày. Chính sách đổi trả